-
科研进展丨我校金大勇团队发表Nature Nanotechnology:营养这样补,才能抗癌!
最新新闻 | 2024-06-12
不受控的快速增殖是肿瘤细胞区别于正常细胞的一个关键特征。近十年来,研究者们逐渐发现,代谢和能量供应的紊乱,是肿瘤快速增殖的最根本原因。因此,肿瘤也被定义为一种代谢疾病,它们重编程新陈代谢,以尽可能为增殖分裂提供足够的物质和能量。在此过程中,一些代谢途径被异常激活,而另一些与增殖无关的代谢途径,则受到抑制。
从癌细胞异常改变代谢出发,研究者们发现了肿瘤治疗的重要靶点。但迄今为止,绝大多数靶向代谢的药物和疗法均聚焦于抑制过度激活的代谢途径。例如,针对糖酵解的HK2抑制剂已在临床上用于治疗各种癌症;芳香化酶抑制剂抑制雌激素合成可对乳腺癌患者有治疗效果。
天之道,损有余而补不足。近日,复旦大学步文博教授团队在学术期刊《自然-纳米技术》上,创新性提出基于纳米技术的肿瘤代谢重激活新疗法。并以黑色素瘤为例揭示:补充特定营养物质重新激活被抑制代谢,同样展现出令人振奋的抗癌效果,并有助于后续的联合治疗。
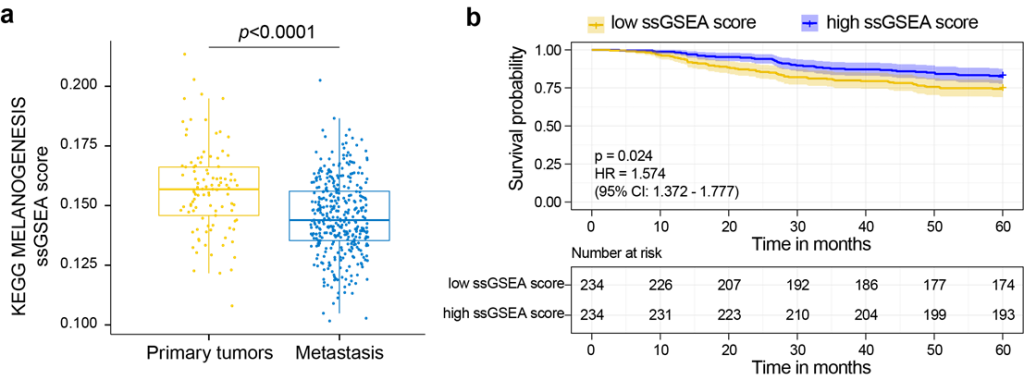
 研究者们首先发现,肿瘤细胞中大多数受抑制的代谢途径,是肿瘤起源组织-细胞类型特异性代谢。例如,皮肤黑色素瘤(SKCM)起源黑色素细胞,合成及分泌黑色素是其重要的功能。而在晚期及转移性SKCM患者中,黑色素合成代谢通路显著下调(图1a),并且与患者生存期负相关(图1b)。
研究者们首先发现,肿瘤细胞中大多数受抑制的代谢途径,是肿瘤起源组织-细胞类型特异性代谢。例如,皮肤黑色素瘤(SKCM)起源黑色素细胞,合成及分泌黑色素是其重要的功能。而在晚期及转移性SKCM患者中,黑色素合成代谢通路显著下调(图1a),并且与患者生存期负相关(图1b)。
而要激活信号通路,通常的方法是筛选关键酶的激活剂,这种方法通常既费时又昂贵;更重要的是,酶激活剂固有的脱靶效,会对机体产生副作用。在该研究中,研究人员将目光投向机体所需的营养物质,如氨基酸、糖类、维生素等,因其可作为天然底物激活特定的代谢途径。如酪氨酸作为黑色素合成的底物,可刺激黑色素合成。值得一提的是,营养物质安全、易得,患者依从性好。然而,小分子营养物质在体内的生物利用度十分有限。
据此,在这项最新研究中,研究人员利用营养物质纳米化的新技术,将酪氨酸制备成靶向黑色素瘤的可降解两亲纳米胶束,利用其与细胞膜的亲和性及肿瘤细胞对纳米材料的包吞作用,克服了细胞对游离酪氨酸摄取的限制,显著提升胞内酪氨酸的含量(图2)。
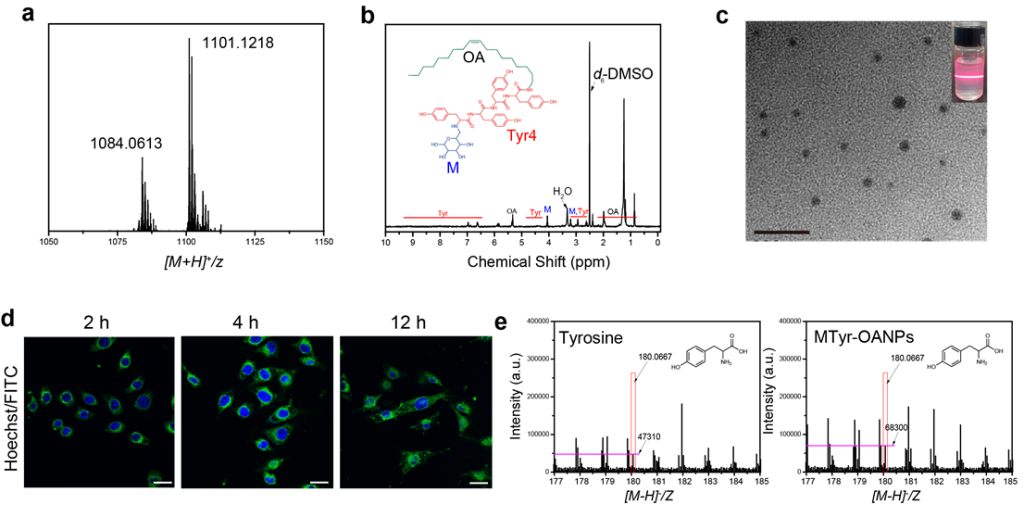
研究发现,酪氨酸纳米胶束通过提高黑色素合成相关酶的活性及表达、促进黑色素小体的合成等途径,激活了黑色素瘤细胞的黑素合成及分泌(较补充游离酪氨酸提高3倍左右)。与此同时,肿瘤细胞增殖也得到了显著抑制。
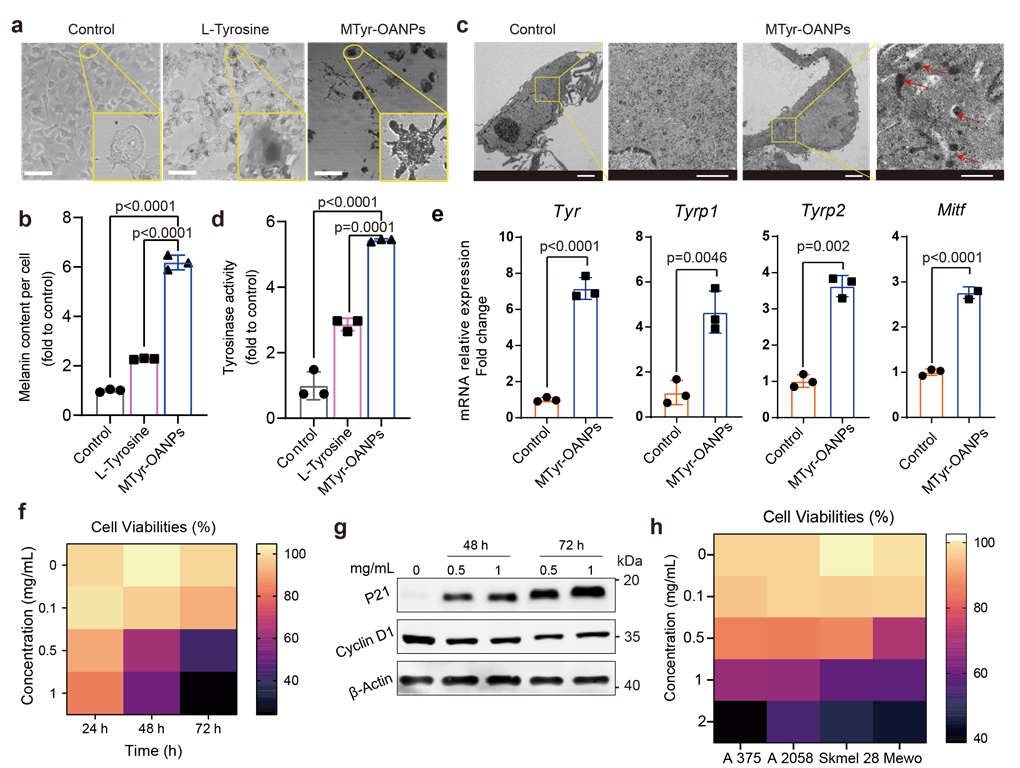
在机制方面,研究人员揭示:黑色素瘤的黑色素合成与糖酵解代谢之间存在相互作用。黑色合成的中间代谢产物5,6-吲哚醌,可以抑制糖酵解关键酶-丙酮酸脱氢酶(PKM)的活性,从而干扰肿瘤糖代谢抑制细胞增殖(图4)。
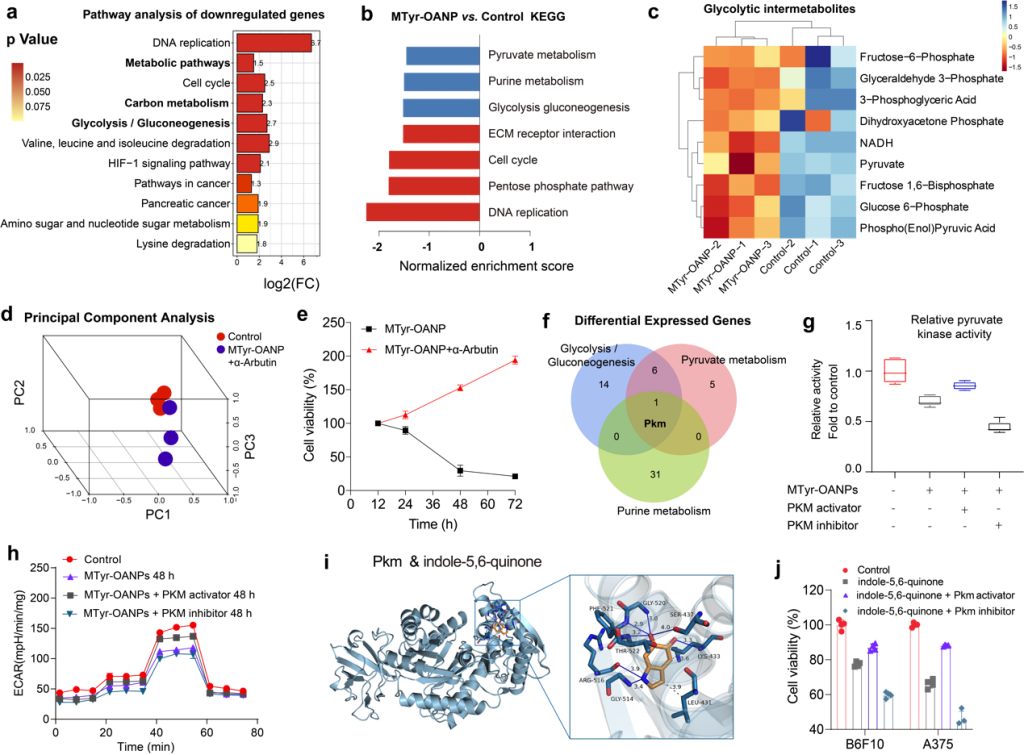
结果显示,酪氨酸纳米胶束在体内可靶向黑色素瘤(靶向效率4.4%),对小鼠和人来源的黑色素瘤(包括BRAF突变型/野生型)都发挥了一定的抗肿瘤作用,且对BRAF野生型肿瘤效果更好(图5)。研究指出,这可能与BRAF突变黑色素瘤中调控黑素合成的转录因子MITF过度泛素化有关,从而为该纳米药物的临床应用提供了科学依据。
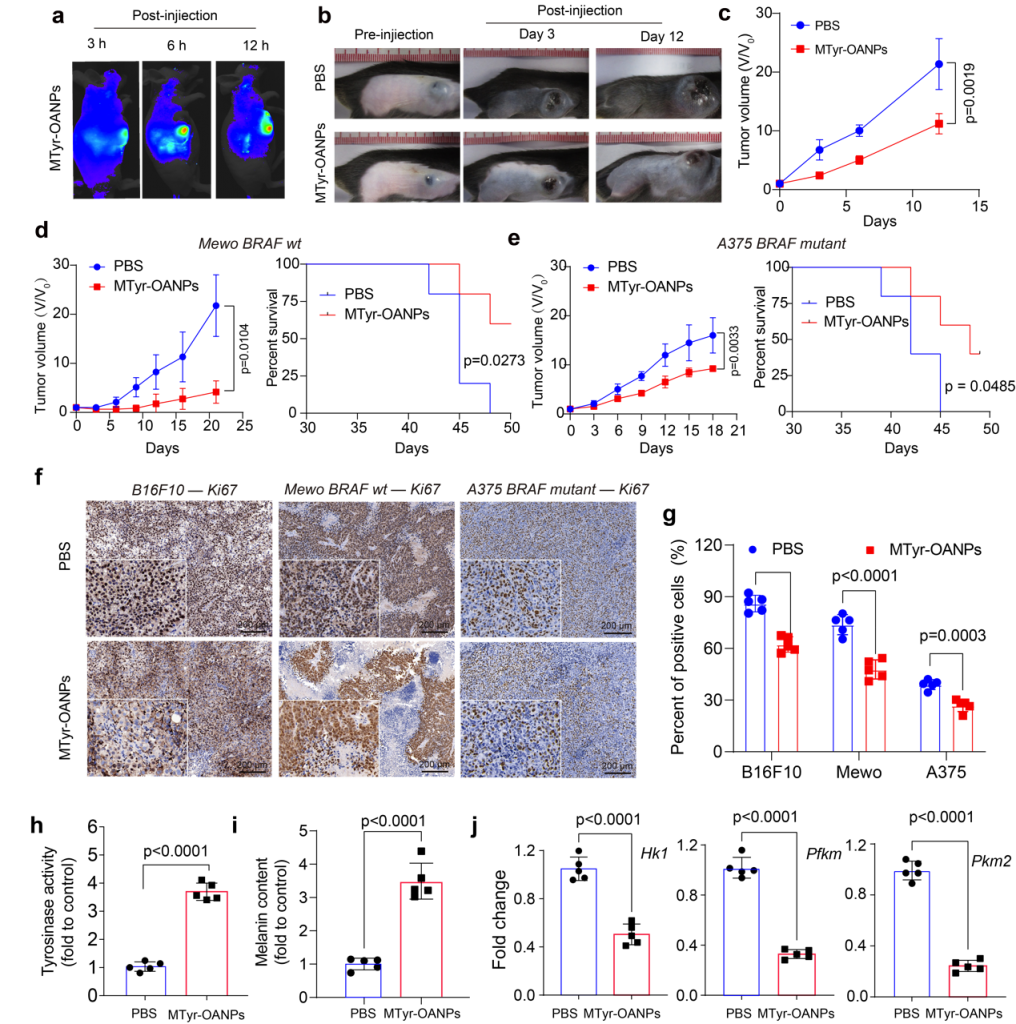
更令人惊喜的是,黑化的黑色素瘤细胞表现出对热应激的抵抗下降。而黑色素作为一种天然的光热试剂,具有优异的光热转化性能。在酪氨酸纳米胶束和近红外光的共同作用下,小鼠黑色素瘤在治疗第6天得到了根除,且在观察的49天内无复发。这说明,重新激活肿瘤代谢通路后在肿瘤内部大量积累的代谢产物和表型重塑,将有助于联合已有治疗手段实现协同抗癌(图6)。
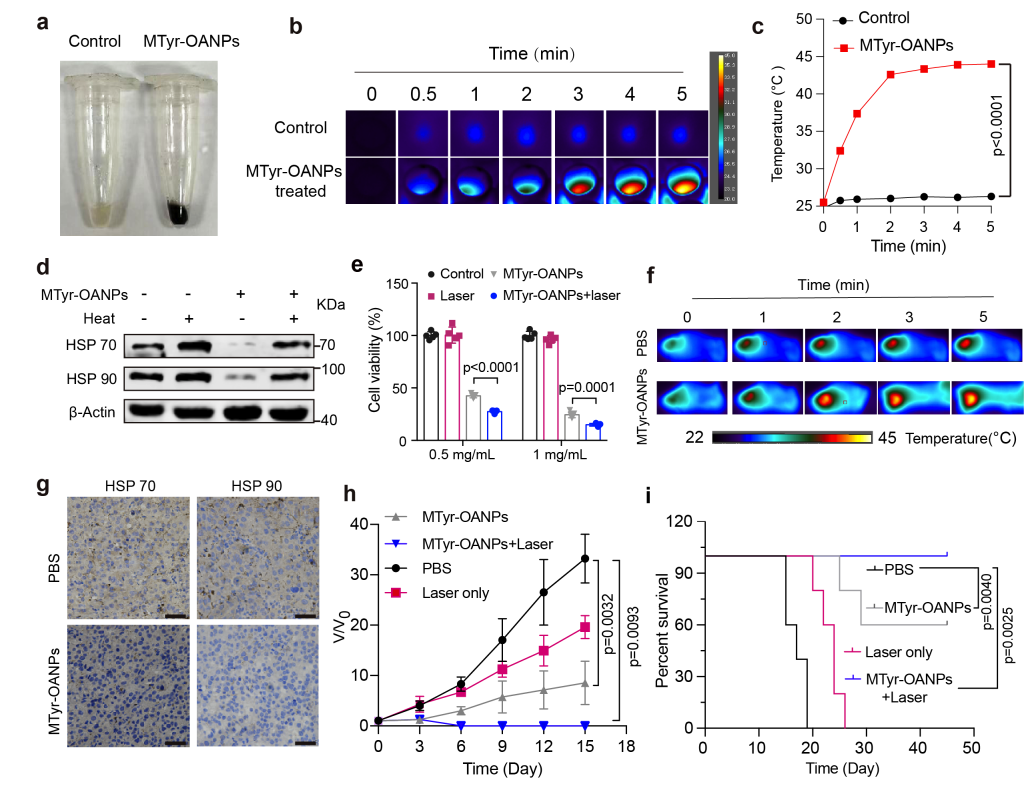
总而言之,这项研究首次提出的基于营养物质纳米化的“代谢重激活”新策略,为肿瘤治疗开辟了新方向和提供了新技术方法;通过揭示被抑制代谢通路与细胞及增殖之间的关系,为肿瘤治疗提供新的靶点;更重要的是,代谢重激活后的肿瘤表型变化和代谢产物积累,可为联合临床已有治疗手段提供新的契机。最后,研究人员指出,他们正在着手其它类型难以根治的实体肿瘤,该疗法和技术有望实现多种肿瘤的特异性代谢治疗!该工作已在线发表于《Nature Nanotechnology》,同济大学生命科学与技术学院助理教授陈杨、同济大学附属第十人民医院副研究员王超超和研究员吴叶林为该论文的共同第一作者;复旦大学材料科学系/聚合物分子工程国家重点实验室步文博教授、宁波东方理工大学(暂名)/澳大利亚悉尼科技大学金大勇院士、复旦大学附属华山医院皮肤科吴金峰教授为论文共同通讯作者。该工作得到了国家自然科学基金、上海市教委创新重大基础项目等经费支持。





